指南共识|食管裂孔疝修补及抗反流手术规范微共识
胃食管反流病(gastroesophageal reflux disease disease, GERD )是常见的消化系统疾病,其发病率有逐年增高的趋势 [1] 。2006 、2007 和 2014 年我国发布了GERD 的内科诊治指南 [2-4] ,2020 年发布了中国胃食管反流 病专家共识,对指导 GERD 的临床诊治发挥了重要作用。近年由于外科手术干预在GERD 的临床实践和研究中的应用,迫切需要国内外科诊疗共识意见来规范治疗,为从事本专业的临床医师提供诊疗纲领,指导相关学科专业医师正确认识和处理此类疾病。该共识列出的报告是来自关于 GERD所发表的文献的系统性回顾和基于明确证据的临床推荐。突出显示了证据的强弱度,没有确凿证据的领域采纳了专家意见。
一、定义及症状
GERD是指胃内容物反流入食管、口腔(包括喉部)或肺所致的症状和并发症 [5] 。GERD 的典型症状是胃灼热和反流,胃灼热指胸骨后烧灼感,反流指胃内容物向咽部或口腔方向流动的感觉。不典型症状有胸痛、上腹痛、上腹部烧灼感及嗳气等。GERD还伴随食管外症状,包括咳嗽、咽喉症状、哮喘和牙蚀症等。对于合并食管裂孔疝的患者,部分合并贫血。
食管裂孔疝是指腹腔内脏器通过膈肌的食管裂孔疝出。多数较小的Ⅰ型(滑动型)食管裂孔疝没有症状。较大的Ⅰ型食管裂孔疝患者可能出现 GERD的症状,其中最常见的是胃灼热、胃内容物反流和吞咽困难。很多Ⅱ、Ⅲ和Ⅳ型(食管旁)疝患者没有症状,或仅有不明确的间歇性症状。最常见的症状是上腹部或胸骨后疼痛、餐后饱胀感、恶心和干呕。与Ⅰ型食管裂孔疝患者相比,此类患者出现GERD 症状的情况较少见。
二、分型
GERD临床上一般分为糜烂性食管炎(erosiveesophagitisesophagitis,EE )或反流性食管炎 reflux esophagitis esophagitis,RE )、非糜烂性食管炎 nonnon-erosive refiux disease disease,NERD)和 Barrett 食管( Barrett esophagus esophagus,BE)三种类型 [7]。食管裂孔疝可大致分为滑动疝和食管旁疝。食管裂孔疝最广义的分类包括4种类型:
Ⅰ型:滑动疝—Ⅰ型或滑动型食管裂孔疝的特征是胃食管连接部移位至膈上。胃仍保持其正常的纵向位置,胃底仍处于胃食管连接部之下。
Ⅱ、Ⅲ、Ⅳ型:食管旁疝 —食管旁疝是有疝囊的真性疝,其特征是胃底经膈食管膜缺损向上疝出。
Ⅱ型食管裂孔疝是由膈食管膜的局部缺损导致的,胃底作为疝的引导点,而胃食管连接部仍固定于主动脉前筋膜和正中弓状韧带。
Ⅲ型食管裂孔疝兼具Ⅰ型和Ⅱ型食管裂孔疝的特征,其特点是胃食管连接部和胃底均经食管裂孔疝出。胃底位于胃食管连接部之上。
Ⅳ型食管裂孔疝与膈食管膜的较大缺损有关,特征是疝囊内存在胃之外的其他器官(如结肠、脾脏、胰腺或小肠) [7]。
三、诊断
诊断治疗标准:(1)有反酸、胃灼热、胸骨后疼痛等典型症状;(2)质子泵抑制剂试验阳性 (3)内镜检查提示反流性食管炎阳性者;(4)24h食管pH监测阳性者;(5)GERDQ量表对胃灼热、反流、上腹痛、恶心、有无睡眠障碍和是否需要服用非处方药物这6项症状在1周内的发作频率进行评分,总分18分,≥8分即可诊断为 GERD [8];(6)高分辨率食管测压(high resolution manometry manometry,HRMHRM)可对整段食管的张力及蠕动收缩情况进行同步监测。有助于明确是否合并食管裂孔疝,能够反映食管的运动功能,为手术方式的选择提供依据 [9] 。通过上消化道内镜检查可能诊断出食管旁疝,但食管吞钡造影才是诊断食管旁疝最敏感的检查。>2cm的滑动型食管裂孔疝可通过食管吞钡造影、内镜检查或食管测压检查得出诊断。相比之下,较小的滑动型食管裂孔疝只能在手术中确诊。CT不被常规推荐,但仍然有助于提供有关食管裂孔疝位置和类型的额外信息。通常,它是在针对不同适应证进行CT扫描时偶然发现的 [10]。
四、治疗策略
GERD的治疗目标包括有效缓解症状、治愈食管炎、提高生命质量和预防并发症。我们强烈建议单纯无症状性Ⅰ型食管裂孔疝无需手术修复。有症状的滑动型食管裂孔疝患者需要同时优先治疗GERD 。无症状食管旁疝患者的最佳治疗方法存在争议。虽然一些专家推荐即使患者没有症状也应进行预防性外科治疗,但也有一些专家反对这样做。存在症状或并发症的食管旁疝(Ⅱ、Ⅲ、Ⅳ型)需要手术修补,是否需要迫切手术取决于起病速度。
紧急修补术的指征包括:急性胃扭转、不能控制出血、梗阻、绞窄、穿孔或继发于食管旁疝的呼吸功能损害。引起急症的食管旁疝死亡率高。
择期修补术的指征包括:存在食管旁疝但症状为亚急性,如吞咽困难、早饱、餐后胸部或腹部疼痛、贫血、呕吐或者内科治疗难以控制的GERD 。手 术修补可改善这些患者的症状和生存质量( quality oflifelife,QOL )[10-11] 。
五、手术方式及要点
1. 手术方式的规范化
规范化抗反流手术可以改善患者手术效果。与任何一个外科操作一样,腹腔镜抗反流手术也受学习曲线的影响,这可能会影响治疗效果。所以,不熟练较高难度腹腔镜手术,尤其是胃底折叠术的外科医师必需在专家指导下完成他们的初期腹腔镜手术,以便减少并发症发病率,提高治疗效果。二次抗反流手术应该由大型三级医学中心的富有经验的外科医师来完成。
2. 胃短血管的切断
根据研究5项随机对照试验的证据显示长达10年随访期间,在生理学、症状学及生活质量等手术结果无差异。而且胃底折叠时切断胃短血管会延长手术时间,增加腹胀和上腹部积气的发病率,减弱胃排气功能。建议胃底能够无张力折叠的情况下需要保留胃短血管。胃底不能能够无张力折叠的情况下要切断胃短血管。
3. 迷走神经的保护
抗反流手术中迷走神经损伤是发生率较高的并发症,虽然迷走神经损伤在短期发生的腹泻、饱食感、吞咽困难及反流等比迷走神经完整者没有差异。但是对于反流症状的长期管理,存在较高的复发率及再手术率,因此我们认为术者手术过程中应谨慎操作尽量保留迷走神经的完整性,尤其是胃-食管反流病患者。在打开小网膜囊,分离右侧膈肌脚过程中应该注意迷走神经肝支的保护以避免增加胆囊结石发生的风险。
4. 食管裂孔的关闭
胃底折叠术中,在食管裂孔缺损较大的情况下应该考虑关闭食管裂孔(缝合膈肌脚),补片修补可能有助于减少折叠疝的发生率。食管前关闭食管裂孔有可能减少术后吞咽困难的发生率,但是稳固此建议需要提供更多证据。在进行 RouxRoux-en -Y胃旁路术、袖状胃切除术和放置可调节胃束带的手术期间,所发现的食管裂孔疝均应进行修复。缝合时建议选用不可吸收单股 聚丙烯缝合线。
5. 补片的应用
应用补片的适应证。(1)巨大型食管裂孔疝,食管裂孔缺损超过5cm ,或超过1/3胃体疝入胸腔;(2)对于膈肌脚发育不良,肌纤维薄弱的患者,单纯缝合修补后,随着呼吸运动及吞咽运动,膈肌脚与横膈的肌纤维容易撕裂,导致食管裂孔疝复发;(3)若患者同时伴有各种慢性疾病(肥胖、便秘、前列腺增生、慢性支气管炎、顽固性呃逆等),易导致腹内压力增高,将腹腔内脏器向食管裂孔处挤压,并通过食管裂孔疝入胸腔 [15] 。
6. 抗反流手术方式的选择
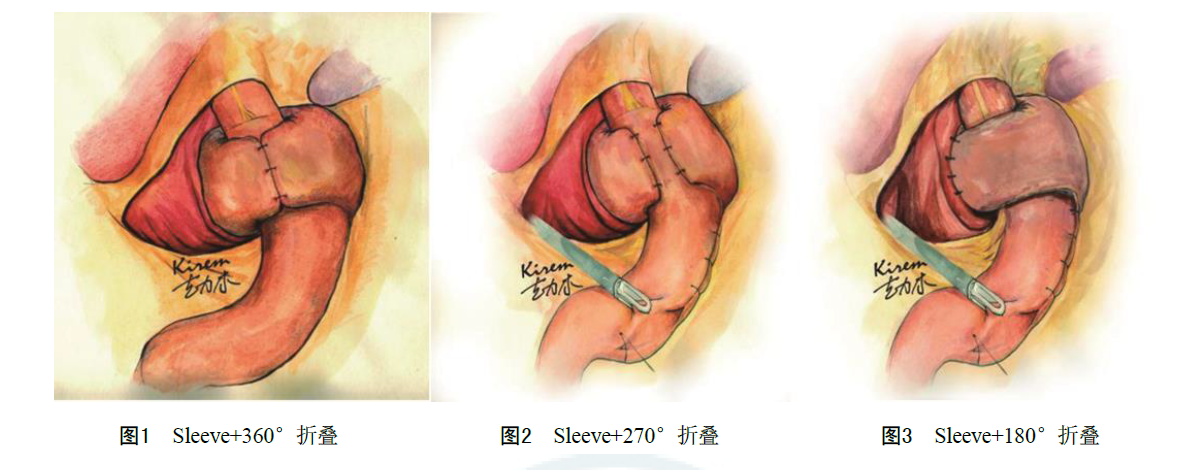
腹腔镜下抗反流手术主要包括 NissenNissen(360°)胃底折叠术 ,ToupetToupet(270°)胃底折叠术 DorDor(180°)胃底折叠术等。见图 1~3。根据现有高质量证据,与完全胃底折叠术比较,部分胃底折叠术后5年的术后吞咽困难发病率、再次手术率低,患者满意度和GERD 控制效果相当。多数文献显示食管前胃底折叠术远期效果并不理想,回顾性研究数据显示部分胃底折叠术的远期效果不如完全胃底折叠术。但是现有证据建议,如果GERD手术由受过相应微创外科训练的外科医师来完成,而且在食管支撑管的配合下采用部分胃底折叠术或短松完全胃底折叠术(1~2cm)可能使术后吞咽困难的发病 率降到最低;采用完全胃底折叠术或较长(至少3 cm)食管后胃底折叠术可能获得最好的治疗效果。
六、肥胖症患者的抗反流手术
由于担心病态肥胖患者(体质量指数>35kg/mm2) 胃底折叠术后失败率较高,以及胃底折叠术无法解决潜在问题(肥胖)及其相关合并症,因此肥胖患者准备实施抗反流手术时,应考虑同时行减肥手术,首选方式是胃旁路手术时应选择联合行袖状胃切除术或直接考虑胃旁路术 [16]。
七、机器人辅助腹腔镜下抗反流手术
虽然机器人辅助可以安全有效地用于胃底折叠术,但与传统腹腔镜检查相比,其成本较高且短期患者预后相似,因此它不是理想的初始选择。然而,在提出更有力的建议之前,需要进一步研究机器人技术的学习曲线和外科医师的工作量 [17]。

